


Duchenne型肌营养不良(Duchenne muscular dystrophy,DMD)是由DMD基因的致病性变异所导致的一种X连锁隐性遗传性肌病。由于DMD为X连锁隐性遗传肌肉病,目前尚无根治手段,对患者及家庭造成严重的心理和经济负担。
有典型的DMD症状和血浆肌酸激酶(creatine kinase,CK)水平升高的男孩应进行基因检测以确认诊断。患者在儿童早期出现活动能力下降,如双下肢无力、鸭步和Gowers’征伴有腓肠肌肥大;随年龄增长,出现双上肢无力及翼状肩胛;晚期可出现关节挛缩及脊柱畸形。血清CK明显升高,
尽管在过去的30年DMD的治疗取得了重大进展,但仍无有效治疗方法。但针对DMD症状的多学科综合管理可以改变疾病的自然病程,提高生活质量和寿命[2]。
Duchenne型肌营养不良(Duchenne muscular dystrophy,DMD)又称为假肥大型肌营养不良 (pseudohypertrophic muscular dystrophy,PMD)、儿童严重全身肌营养不良(severe generalized muscular dystrophy of childhood),是由DMD基因致病性变异所导致的一种X连锁隐性遗传性肌病。患者多在2~3岁左右出现蹒跚学步、爬楼梯困难和频繁跌倒,逐步丧失活动能力,最终累及呼吸肌,需要呼吸机辅助通气,并最终死于心力衰竭和/或呼吸衰竭。在精心护理下,多数DMD患者寿命可达到40岁左右[1-4]。
由于DMD为X连锁隐性遗传肌肉病,目前尚无根治手段,对患者及家庭造成严重的心理和经济负担。女性携带者通常没有症状,约2.5~19%会出现骨骼肌无力,7.3~16.7%会合并
DMD全球各地区发病率大致相同[2],在我国男孩发病率约为1/4560[5]。女性DMD患者罕见,发病率小于1/100万,且均合并
DMD基因定位于Xp21.2-p21.1区域,全长约2.4Mb,是迄今为止发现的人类最大基因,包含有79个外显子和78个内含子,编码3685个氨基酸,组成427kD的细胞骨架蛋白-抗肌萎缩蛋白(dystrophin)。目前已经发现了数千种不同的DMD基因突变,大约60~70%的DMD患者的突变为大片段缺失,20%为点突变、小片段缺失或插入,5~15%为片段重复[2]。DMD基因的外显子45~55和3~9为突变的热点区,分别占比为47%和7%[7, 8]。少数患者为X染色体和常染色体易位致病[9]。
抗肌萎缩蛋白主要位于骨骼肌和心肌细胞膜的质膜面,具有细胞支架、抗牵拉、防止肌细胞膜在收缩活动时撕裂的功能。
作为细胞骨架的主要成分,抗肌萎缩蛋白与肌膜、细胞骨架(肌动蛋白微丝、中间丝、微管和其他相关结构蛋白)、通道蛋白和支架蛋白直接或间接地相互作用,并和肌纤维膜上的多种糖蛋白结合为抗肌萎缩蛋白相关蛋白复合体(dystrophin-associated protein complex,DAPC)。这些复合体可与基膜层粘连蛋白连接,以维持肌纤维的稳定性。
由于DAPC在维持肌肉细胞结构完整性和收缩活性方面具有重要的机械和信号传导作用,DMD患者细胞内缺乏正常的抗肌萎缩蛋白,导致DAPC结构异常,对肌纤维功能产生广泛影响。
此外,肌肉收缩引起的机械损伤[2, 10-12]、局部微循环障碍[2, 13, 14]、氧化自由基损伤[2, 15-17]、胞质内钙超载[2, 18]均参与疾病的生理过程,共同造成肌纤维变性、坏死。
由于抗肌萎缩蛋白的表达异质性以及DAPC的组织差异性,心脏组织受累较骨骼肌轻,故症状出现较晚[2]。
在大脑中,抗肌萎缩蛋白在杏仁核、海马和小脑浦肯野细胞的突触后抑制性γ-氨基丁酸(γ-aminobutyric acid,简称GABA)能神经元中表达[19, 20],因此DMD基因突变也会引起中枢神经系统症状。
约三分之一的DMD患者存在认知障碍、注意力下降、学习困难和精神行为异常[21]。认知障碍虽然在疾病早期出现,但进展缓慢[2]。
有典型的DMD症状(详细见下一章节“问诊和症状”)和血浆肌酸激酶(creatine kinase,CK)水平升高的男孩应进行基因检测以确认诊断。
首选多重连接探针扩增技术(multiplex ligation-dependent probe amplification,MLPA)或比较基因组杂交技术(comparative genome hybridization,CGH),若发现DMD基因重复、缺失,则DMD诊断成立。
若未发现明确致病突变或存在微小突变,应进行一代测序(Sanger法测序)或外显子靶向捕获二代测序技术。
若仍未发现致病突变,应进行肌肉活检、蛋白质组学或转录组学分析[2, 3, 5]。
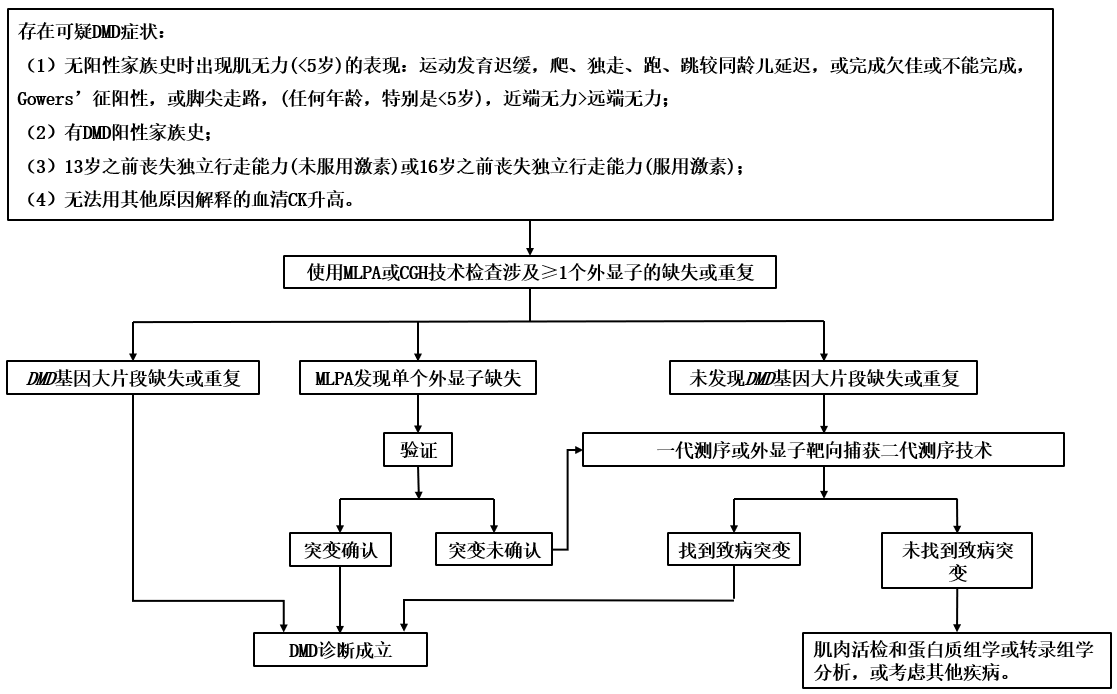
图1 诊断流程图[2, 3]
DMD起病较为隐匿,患者往往以活动能力下降为首发症状,因此问诊需仔细询问患者的主要症状、发病形式、伴随症状,注意症状出现的先后顺序和演变情况,以及其他器官系统损害的症状,阳性症状以及重要的阴性症状,同时注意询问家族史,对诊断的确立至关重要。
DMD病情进展可分为五个阶段,分别是症状前期、早期独走期、晚期独走期、早期不能独走期以及晚期不能独走期[3, 5]。
各期典型症状详细描述见表1。
表1 DMD各期典型症状

DMD为全身性疾病,因此查体应尽量全面:
1. 一般查体
注意体格发育(身高和体重)、智力发育、性征发育以及全身营养状况,患者可有身材矮小,注意力缺陷障碍。
2. 内科/外科查体
包括心脏、肺、骨、关节的检查,患者可能出现
3. 神经系统专科查体
包括意识状态、高级神经功能、颅神经、运动系统、感觉、反射、脑膜刺激征以及自主神经检查。
患者骨骼肌可出现假性肥大,触之坚韧。
Gowers’征阳性——患儿自仰卧位起立时,必须先翻身转为俯卧位,依次屈膝关节和髋关节,并用手支撑躯干成俯跪位,然后以两手及双腿共同支撑躯干,再用手按压膝部以辅助股四头肌的肌力,身体呈深鞠躬位,最后用手支扶小腿并逐渐上移至股部,将身体重力支于手臂,而后挺起腰部而直立,因用力而出现面部发红。
建议优先选择如下必要的辅助检查,以明确疾病的诊断:
需完善血常规、肝肾功能、CK、乳酸脱氢酶(lactate dehydrogenase,LDH)、肌酸激酶同工酶(creatine kinase muscle and brain isoenzyme,CK-MB)、肌红蛋白(myoglobin,Mb)等检测。
多数患者可发现血清CK明显升高(约20~100倍)[1, 2, 4]。在疾病进展期,可以出现转氨酶升高,但需注意在晚期肌肉变性严重,血清CK可能正常甚至下降[1]。
DMD患者针极
首选MLPA或CGH进行大片段缺失或重复致病性变异检测,对于未发现大片段缺失或重复致病性变异的患者,应进行一代测序或外显子靶向捕获二代测序技术。若仍未发现致病性变异的患者,应行肌肉活检、信使核糖核酸(messenger ribonucleic acid,mRNA)分析进一步寻找致病性变异[2, 4]。
1.在基因检查不能明确诊断以及出现未报道的新突变时应进行肌肉活检和抗肌萎缩蛋白分析[22],针对抗肌萎缩蛋白抗体进行骨骼肌免疫组织化学染色。
2.需注意抗肌萎缩蛋白的表达降低也可见于肌聚糖蛋白病[28],而抗肌萎缩蛋白的表达异常也可导致肌聚糖蛋白的表达异常,因此需要同时进行抗肌聚糖蛋白的免疫染色和结合基因检查结果进行分析[5]。
DMD典型的免疫组织化学染色表现为:肌纤维膜抗肌萎缩蛋白-羧基端(C端)结构域为阴性 [23-25],抗肌萎缩蛋白-氨基端(N端)结构域为阴性或几乎阴性,抗肌萎缩蛋白-杆状区(R端)结构域通常有一定的表达,可伴有个别突变修复肌纤维[26, 27]。
患者的头颅核
肌肉MRI可以评估骨骼肌病变的严重程度,协助DMD的早期诊断和进行随访。
在疾病早期,大腿臀大肌和大收肌即可出现不同程度的脂肪浸润和
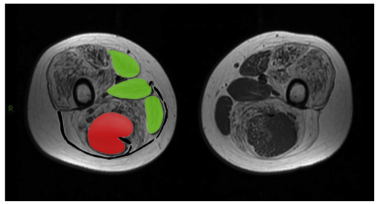
图2 “三叶一果”征(图片引自:Zheng Y, Li W, Du J, et al. The trefoil with single fruit sign in muscle magnetic resonance imaging is highly specific for dystrophinopathies[J]. Eur J Radiol, 2015, 84 (10): 1992-1998. )
注:DMD患者肌肉MRI可见缝匠肌、股薄肌、长收肌和半腱肌轻度或无脂肪浸润,其余肌肉受累严重
常规心电图、
基因检查发现了意义不明的突变,或未发现致病突变,或怀疑表观遗传学影响患者DMD基因表达时,可进行转录组学研究,评估DMD基因表达情况[31, 32]。
为详细评估患者病情,情况允许建议完善如下辅助检查:
肺功能检查可以详细评估患者肺活量、呼吸功能储备,如患者具有夜间通气不足的症状,如早晨
DMD后期会出现肢体肌肉挛缩、关节畸形和脊柱侧弯,建议完善包括脊柱全长正侧位X光检查、电子计算机断层扫描(computed tomography,CT)检查等影像学检查,以及
包括身高、身体质量指数(body mass index,BMI)、尺骨长度及骨龄、甲状腺功能、垂体激素等[5],有助于评估患者是否存在生长发育迟滞。
DMD患者需神经心理学评估,评估患者智力、认知功能、语言功能,以及情绪量表、缺陷-多动障碍评估表等[5]。
至今已经发现了许多对DMD有潜在意义的生物标志物,有些反映了肌纤维变性、坏死,如DMD患者肌纤维miR-1、miR-29C、miR-135a含量减少[34],而血清miR-1、miR-206、miR-133、miR-499、miR-208a、miR-208b含量增加[35],以及尿中的肌红蛋白N片段增加等[36];有些反映肌纤维继发纤维结缔组织增生,如血清白细胞介素-13、转化生长因子-β的含量变化等[37]。此外还有反映DMD相关的炎症和氧化应激反应:如DMD患者肌纤维和血清细胞因子如肿瘤坏死因子、白细胞介素-6、γ-干扰素含量升高[37],骨桥蛋白升高等[38]。以上有些检查目前停留在研究阶段,临床应用较少,随着研究深入,将逐步应用到临床。
患者在儿童早期出现活动能力下降,如双下肢无力、鸭步和Gowers’征伴有腓肠肌肥大;随年龄增长,出现双上肢无力及翼状肩胛;晚期可出现关节挛缩及脊柱畸形。血清CK明显升高,
DMD常见并发症包括呼吸系统并发症、心脏并发症、骨及关节并发症。
1.呼吸系统并发症
多数患者20岁左右出现呼吸肌无力以及相关并发症,如肺部感染、呼吸衰竭等。肺部影像学检查、痰液细菌学检查以及血生化检查有助于检测肺部感染;肺功能、
2.心脏并发症
常规心电图、24小时动态心电图有助于对心脏进行电生理评估,
3.骨及关节并发症
DMD患者常因跌倒发生上肢和下肢骨折[39],因使用
DMD患者常合并脊柱侧弯,脊柱全长正侧位X光检查可判断患者脊柱弯曲程度。关节X光、CT或MRI有助于诊断关节挛缩。
包括Becker型肌营养不良症(Becker muscular dystrophy,BMD)、肢带型肌营养不良症(limb-girdle muscular dystrophy,LGMD)等。BMD临床表现与DMD相似,但程度较轻,疾病进展慢,预后相对好[2-4]。LGMD为常染色体隐性或显性遗传,常10~20岁起病,首发症状多为骨盆带肌肉萎缩、腰椎前凸、鸭步,下肢近端无力,可有腓肠肌假性肥大,逐渐累及上肢近端,抬臂困难、翼状肩。
血清CK明显升高,
脊肌萎缩症II型(spinal muscular atrophy II,SMAII)即慢性Werdnig-Hoffmann病,呈对称分布的四肢近端肌萎缩、肌束震颤,该病起病较DMD早(1岁半前起病)。
血清CK基本正常,
血清CK明显增高。
易误诊人群
DMD为X连锁隐性遗传性肌病,患儿多在2~3岁左右出现活动能力下降,程度较轻,容易被忽略。DMD女性患者罕见,常常被误诊。
本病被误诊为其他疾病
DMD易误诊为其他类型肌营养不良,如BMD、LGMD;其他类型肌肉病如脂质沉积性疾病、糖原沉积性肌病、肌炎等。
其他疾病被误诊为本病
其它类型的肌营养不良、炎性肌病、其他代谢性肌病等易被误诊为本病。
避免误诊的要点
详细询问患者病史,尤其注意观察患者的活动能力,仔细的查体,以及神经系统、心脏、呼吸系统、骨及关节的辅助检查,结合基因检测,可最大限度减少误诊。
(一)一级预防
由于DMD目前尚无有效的治疗方法,因此,避免患病胎儿出生对于疾病的预防显得尤为重要。首先,应确定DMD患者的基因型,然后确定其母亲是否是携带者。当携带者怀孕需进行产前基因诊断,与先证者相同突变基因的男胎应采取人工流产措施;携带有与其母亲相同突变基因的女胎,也应告知受检夫妇,因8%左右的女性携带者出现轻重不同的症状,而且其下一代男孩仍将有发病风险[4]。需注意因基因突变可能发生在卵细胞内,因此已生育过1个DMD患儿的母亲,即使不是携带者,当再次怀孕后也应做产前基因诊断[2]。
(二)二级预防
DMD为X连锁隐性遗传性肌病,避免患病胎儿出生是减少后代发病最为有效的手段。患儿一旦出生,将不可避免地出现进行性肌肉变性坏死的症状,目前无有效的二级预防措施。
DMD一旦发病,肌肉变性、坏死将持续性进展。在独走期的任何阶段都有摔倒风险,晚期独走期应提供辅助站立与行走设备,增加骨折预防措施。每周进行4~6次维持关节活动范围的康复治疗,包括对上下肢各关节活动度下降。可使用关节矫形器将关节维持在中立位,延缓关节挛缩畸形;站立困难的患者可以使用被动及主动辅助站立装置,晚期独走期和不能独走期患者可以使用膝-踝-足矫形器;应为不能独走期患者提供定制的座椅、轮椅等设备,以帮助患者尽可能独立地完成日常生活相关的活动。
DMD患者一旦确诊,需要长期随访,复诊和随访内容应个体化制定方案,已出现功能损害的器官应加强随访频率,尚未出现功能损害的器官,应每年随访。
1.患者教育:DMD为X连锁隐性遗传性肌病,目前无特效的治疗手段,建议生育过DMD患儿的基因携带者进行产前咨询、优生优育。
2.改变生活和饮食习惯:DMD患者应当多晒太阳、进食富含维生素D和钙的高氨基酸饮食,预防过度
3.需要向患者及其家属普及的急救知识:遇到突发事件(如心脏事件、
本站内容仅供医学专业人士参考
不能作为诊断及医疗依据,请谨慎参阅
©医知源 版权所有,未经许可,不得以任何形式对医知源内容和插图进行转载使用。



 长按文字
长按文字