


低钾型周期性麻痹(hypokalemicperiodic paralysis)又称低钾型周期性瘫痪,一种常染色体显性遗传或散发的疾病,我国以散发多见。
患者的临床表现为发作性肌无力、血清钾降低、补钾后能迅速缓解症状;为周期性瘫痪中最常见的类型。低钾型周期性瘫痪会导致患者反复出现肢体瘫痪,部分患者肌酶明显增高,少数患者心律失常,甚至引起死亡[4]。
具体发病机制尚未明确,但可能与骨骼肌细胞膜内外钾离子浓度的波动有关。
早发现、早诊断、积极纠正
低钾型周期性麻痹(hypokalemicperiodic paralysis)又称低钾型周期性瘫痪,一种常染色体显性遗传或散发的疾病,我国以散发多见。
患者的临床表现为发作性肌无力、血清钾降低、补钾后能迅速缓解症状;为周期性瘫痪中最常见的类型。
低钾型周期性麻痹又分为原发性和继发性两类。在原发性低钾型周期性麻痹中,又包括家族性和散发性两种形式。家族性低钾型周期性麻痹多见于西方国家,在我国则以散发病例为主[1]。
继发性最常见于甲亢性低钾型周期性麻痹,还见于
原发性低钾型周期性麻痹则是一种常染色体显性遗传的离子通道型肌病。
这种疾病的主要临床特点是反复发作的肌无力伴有血清钾的降低。首次发作多见于10~30岁,持续时间数小时至数天,发作的频率不等。
此外,摄取大量的碳水化合物、剧烈的运动以及受凉感冒等因素容易诱发该病[2]。
低钾型周期性瘫痪会导致患者反复出现肢体瘫痪,部分患者肌酶明显增高,少数患者心律失常,甚至引起死亡[4]。
原发性低钾型周期性瘫痪发病率为1/10万,男性多于女性,文献报道男性约占62%,女性约占38%[1]。
一项对1366名我国甲状腺毒性患者的研究显示,其中1.8%的患者有低钾型周期性瘫痪病史。
尽管甲状腺毒症在女性中比男性更普遍,但是男性中甲亢继发低钾型周期性瘫痪的发病率是女性的22~76倍[3]。
原发性低钾型周期性瘫痪是一种常染色体显性遗传的疾病,其致病基因主要由位于1号染色体长臂(lq31-32),这个基因负责编码肌细胞中的二氢吡啶敏感L型钙离子通道(L type calcium channel)蛋白,它是二氢吡啶复合受体的一部分,位于横管系统中,通过调控肌质网钙离子的释放影响肌肉的兴奋-收缩偶联[5,6]。
肌无力在餐后或剧烈运动后的休息期间最容易发作。另外,能够促使钾离子进入细胞内的因素,例如注射胰岛素、肾上腺素或大量的葡萄糖,也能诱发[7]。
常见诱因:疲劳、饱餐、寒冷、酗酒、精神刺激等。
具体发病机制尚未明确,但可能与骨骼肌细胞膜内外钾离子浓度的波动有关。正常情况下,钾离子浓度在肌膜内高,肌膜外低,当两侧维持这种正常比例时,肌膜才能保持正常的静息电位,才能对乙酰胆碱(ACh)的去极化产生正常反应。然而,患者的肌细胞膜经常处于轻度去极化状态,稳定性较差,电位稍有变化即产生钠离子在膜上的通路受阻,导致电活动的传递障碍。在疾病发作时,受累肌肉对一切电刺激不产生反应,处于瘫痪状态[8,9,10]。
低钾型周期性瘫痪的诊断流程见图1。
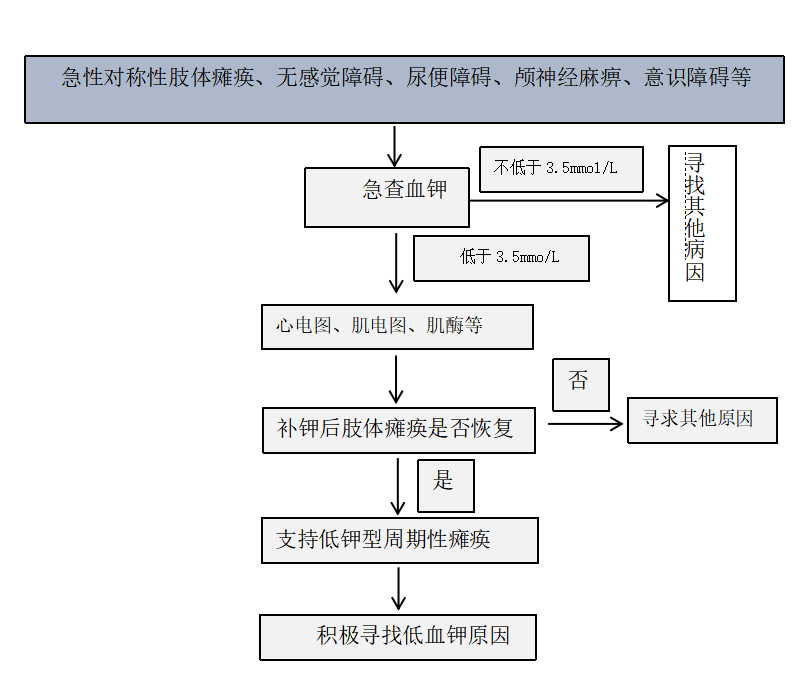
图1 低钾型周期性瘫痪的诊断流程[1,10]
起病方式是否为急性发病;肢体无力是否为对称性,有无伴随感觉障碍、
既往有无类似肌无力发作史。
有无家族史。
发病前有无诱因:如感染、疲劳、饱餐、酗酒、精神刺激等;有无甲状腺功能亢进、醛固酮增多症、肾衰竭等病史,服药史(如利尿剂等)。
突发四肢迟缓性瘫痪,一般下肢重于上肢,近端重于远端。
可伴有肢体酸胀和针刺感的症状。通常来说,脑神经支配的肌肉一般不受累,膀胱直肠括约肌的功能很少受累。在少数严重的病例中,可能会出现呼吸肌麻痹、尿便潴留、心动过速或过缓、心律失常、血压下降等情况甚至会危及患者的生命。
生命体征(血压、呼吸、心率、体温),有无
1.阳性体征
对称性的肢体弛缓性瘫痪、下肢通常比上肢更为严重,近端重于远端。患者的瘫痪肢体肌张力会降低,腱反射也可活跃甚至亢进、可伴肢体肌肉压痛阳性。
2.阴性体征
无
在发病期间,患者的血清钾常常会低于3.5mmol/L。根据具体数值,我们可以将其分为轻度下降(3~3.5 mmol/L)、中度下降(2.5~3.0 mmol/L)以及重度下降(<2.5 mmol/L)。在发作期间恢复正常。
心电图会显示出典型的低钾性改变,包括出现U波、T波低平或倒置、P-R间期和Q-T间期延长、ST段下降以及QRS波增宽。
血常规、尿常规、甲状腺功能、肝肾功能、血糖、糖化血红蛋白、二氧化碳结合力、血醛固酮等检查。
明确有无继发性周期性瘫痪。
低钾型周期性麻痹可表现为运动电位时限短、波幅低,完全性瘫痪时运动单位电位消失,电刺激无反应。膜静息电位低于正常。
表现为感觉、运动神经远端潜伏期延长、传导速度减慢,F波可见潜伏期延长或出现率下降,提示周围神经存在脱髓鞘性病变。
主要用于鉴别诊断,如急性格林巴利综合征。
可行CACNAIS、SCN4A、KCNE3基因突变筛查。
此基因学检查阴性不能完全排除原发性低钾型周期性麻痹,可能存在未知的疾病相关基因[11]。
1.常染色体显性遗传或散发。
2.突发四肢弛缓性瘫痪,近端为主,无
3.数小时至一日内达高峰。
4.血清钾低于3.5mmol/L,心电图呈低钾性改变。
5.经补钾治疗后肌无力迅速缓解[12]。
若血清钾低于2.5mmol/L(重度低钾),需警惕因严重低钾导致
1.心律失常
心电图或心电监护即可明确诊断。
2.麻痹性肠梗阻
腹胀、肠鸣音减弱或消失,腹部DR或CT无机械性肠梗阻征象,补钾后腹胀等肠梗阻症状明显缓解。
3.呼吸肌麻痹
胸闷、气喘不适,血气分析提示呼吸衰竭。
通常在10岁以前发病,白天运动后的发作频率较高。肌无力症状持续时间较短。
发作时血钾升高,心电图异常提示高血钾的改变,可以自行缓解,或通过降血钾治疗得到改善。
较罕见,通常在10岁前发病,常在夜间发作。肌无力症状持续时间较长,无肌强直表现。
血钾正常,补钾后症状可能加重,服用钠后症状减轻。
可以是亚急性或慢性隐匿起病,可累及四肢和脑神经支配的肌肉。症状有波动性,晨轻暮重,病态疲劳。
疲劳试验和新斯的明试验阳性。血清钾正常,重复神经电刺激低频、高频均有波幅递减,抗乙酰胆碱受体等抗体阳性可以用于鉴别。
表现为四肢弛缓性瘫痪,远端重于近端,可有周围感觉障碍和脑神经损害。
脑脊液中蛋白-细胞分离现象,
易误诊人群
老年人:尤其是合并有多种基础疾病的老年人,因临床症状不典型,且容易被其他基础疾病的临床症状干扰[14]。
本病被误诊为其他疾病
1.吉兰-巴雷综合征。
2.继发性低血钾。
3.
其他疾病被误诊为本病
1.继发性低血钾。
2.吉兰-巴雷综合征。
3.
避免误诊的要点
要重点掌握低钾型周期性麻痹临床特点避免误诊。(见诊断标准)
1.对发作频繁者,发作间期可口服钾盐1g,tid;螺内酯200mg,bid,以防发作。
2.避免各种发病诱因如避免过度疲劳、受凉及精神刺激,低钠饮食,忌摄入过多高碳水化合物等。
该病经积极治疗后一般均能快速缓解,一般无需特殊康复治疗。
定期复查血钾,尤其是出现肌无力症状,需及时复查血钾。
1.避免各种发病诱因如避免过度疲劳、受凉及精神刺激,低钠饮食,忌摄入过多高碳水化合物及酒精、尽量避免服用排钾利尿剂等。
2.定期复查血钾,尤其是出现肌无力症状,需及时复查血钾,及时发现及时纠正[20]。
本站内容仅供医学专业人士参考
不能作为诊断及医疗依据,请谨慎参阅
©医知源 版权所有,未经许可,不得以任何形式对医知源内容和插图进行转载使用。



 长按文字
长按文字