



根据第四版“全球心肌梗死定义”标准,急性心肌梗死(AMI)是指在急性心肌损伤【血清心脏肌钙蛋白(cardiac troponin,cTn)增高和/或回落的基础上,至少有一次高于正常值上限(参考值上限值的99百分位值)】,同时,还需要存在急性心肌缺血的临床证据。
根据心电图表现,AMI分为ST段抬高型心肌梗死(STEMI)和非ST段抬高型心肌梗死(NSTEMI)。
STEMI的初诊通常基于持续性心肌缺血的症状、体征以及标准12导联或18导联心电图检查。当临床症状怀疑心肌梗死,且心电图ST段抬高时,应尽快启动再灌注治疗程序,不要因为等待cTn的检测结果而耽误再灌注治疗的时机[8]。
根据第四版“全球心肌梗死定义”标准,急性心肌梗死(AMI)是指在急性心肌损伤【血清心脏肌钙蛋白(cardiac troponin,cTn)增高和/或回落的基础上,至少有一次高于正常值上限(参考值上限值的99百分位值)】,同时,还需要存在急性心肌缺血的临床证据,包括:
① 出现急性心肌缺血的症状。
② 出现新的缺血性心电图改变。
③ 出现新的病理性Q波。
④ 出现新的存活心肌丢失或室壁节段运动异常的影像学证据。
⑤ 冠状动脉造影或腔内影像学检查或尸检证实存在冠状动脉血栓形成。
根据心电图表现,AMI分为ST段抬高型心肌梗死(STEMI)和非ST段抬高型心肌梗死(NSTEMI)。
STEMI在年轻人(年龄<60岁)中发病率较老年人高,男性发病率高于女性[1]。
近期研究数据表明,STEMI相关不良事件发生率正在逐渐下降,可能与再灌注治疗,包括经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)、溶栓治疗(thrombolytic therapy)和急诊冠状动脉旁路移植术(coronary artery bypass grafting,CABG),抗栓治疗以及有效的二级预防有关。
尽管如此,STEMI的死亡率仍然较高,欧洲心脏病学会(ESC)注册研究显示,不同国家STEMI患者住院期间死亡率为4%至12%,血管造影注册研究显示STEMI患者第一年死亡率约为10%[2-4]。
STEMI是冠状动脉粥样硬化性心脏病(CAD)的一种严重类型,有较高的病死率(mortality)和病残率(morbidity)。
STEMI的病死率受多种因素影响,如年龄、Killip心功能分级、得到治疗前延误时间、相关急救系统的完善程度、治疗策略、既往心肌梗死病史、糖尿病病史、肾功能情况、病变冠状动脉数量及左心室射血分数等。
《中国心血管健康与疾病报告2020》显示,2001~2011年因AMI住院的患者中,STEMI占86.0%,农村地区AMI病死率大幅超过城市。发病12h内到达医院的STEMI患者有70.8%接受再灌注治疗。县级医院的再灌注治疗率明显较低,再灌注治疗的延迟仍然比较明显,只有约1/3的患者能在指南规定时间内得到再灌注治疗;省级、地市级和县级医院STEMI患者院内病死率依次递增(分别为3.1%、 5.3%和10.2%)[5]。
女性发生CAD的平均年龄较男性晚7~10年,但心肌梗死仍为女性致死的主要原因。60岁以下的人群中,女性心肌梗死预后是否较男性不良尚存争议,但研究表明,男性和女性经再灌注治疗和二级预防获益相当,应接受同样的管理策略[6]。
已有明确循证医学证据CAD的危险因素包括:年龄、男性、高血压、吸烟、血脂异常、糖尿病、早发冠心病家族史(一级亲属男性<55岁、女性<65岁确诊冠心病)。
其他可能的冠心病危险因素还包括
AMI的病理基础是冠状动脉粥样硬化,STEMI的发生则是由于在冠状动脉内不稳定的斑块破裂、糜烂或侵蚀基础上,激活血小板和凝血系统,继发血栓形成,导致冠状动脉完全闭塞,心肌的血供显著减少或完全中断,导致心肌严重、持久的急性缺血,从而引发心肌细胞的损伤和坏死。在心肌缺血和缺氧的情况下,葡萄糖酵解程度增加,产生大量乳酸,导致局部心肌细胞发生酸中毒。
另外,与正常的有氧分解相比,糖酵解只能产生较少的ATP,无法提供足够的能量满足心肌代谢需求。ATP不仅是心肌收缩的能量来源,也是推动钠泵和钙泵的动力。心肌缺血可影响心肌的收缩和舒张功能,在血液动力学上,表现为心排血量降低,左心室充盈压升高,严重时临床表现为心力衰竭和
从病理角度看,心肌的形态学变化呈动态演变。梗死灶一般在血流中断6小时后肉眼才能辨认,呈苍白色,8~9小时后成土黄色。光镜下,心肌纤维早期凝固性坏死,核碎裂、消失,胞质均质红染或呈不规则粗颗粒状,即“收缩带”,细胞间质
一般情况下,心肌梗死后30分钟心肌细胞内糖原减少或消失。心肌细胞受损后,肌红蛋白迅速从心肌细胞溢出入血,6~12小时达到峰值。心肌细胞内的cTn、谷草酸-草酰乙酸转氨酶(SGOT)、谷氨酸-丙酮酸转氨酶(SGPT)、肌酸磷酸激酶(CPK)和乳酸脱氢酶(LDH)透过损伤的细胞膜释放入血。
若大块心肌梗死累及心室壁全层,则病理上呈透壁性心肌梗死,在心电图上相继出现ST段抬高、病理性Q波及T波倒置,即STEMI患者心电图的“动态演变”[9]。
通常是在冠状动脉不稳定斑块破裂、糜烂、侵蚀及内皮损伤基础上继发血栓形成,导致冠状动脉急性、持续性、完全闭塞,血供显著减少或中断,使对应的心肌严重而持久地急性缺血,从而导致心肌细胞损伤及坏死。
STEMI的初诊通常基于持续性心肌缺血的症状、体征以及标准12导联或18导联心电图检查。当临床症状怀疑心肌梗死,且心电图ST段抬高时,应尽快启动再灌注治疗程序,不要因为等待cTn的检测结果而耽误再灌注治疗的时机[10]。
STEMI缺血性
除了
少数患者可能没有明显的
由于坏死物质的吸收,可以引起
大部分在疼痛发生24~48小时内出现,程度与梗死范围呈正相关,体温一般在38℃左右,一般不会超过39℃,持续时间约1周。
剧烈的疼痛常伴有频繁的恶心、呕吐和上腹胀痛。这与迷走神经受到坏死心肌刺激、心排血量降低和组织灌注不足等因素有关。同时,肠胀气也是常见的症状,重症患者可能会出现呃逆。
在疼痛期间,血压下降是常见的,但不一定表示休克。
如果疼痛减轻后,收缩压仍然低于80mmHg,并伴有烦躁不安、面色苍白、皮肤湿冷、脉细而快、大汗淋漓、尿量减少(<20ml/h)、神志迟钝甚至
休克多在发病后的几小时至几天内发生,大约有20%的AMI患者会出现休克,主要是心原性,由于心肌广泛坏死(超过40%)导致心排血量急剧下降所致。神经反射引起周围血管扩张是次要因素,有些患者可能还存在血容量不足的因素。
应密切注意患者生命体征:观察患者的一般状态,有无皮肤湿冷、面色苍白、烦躁不安、颈静脉怒张等,听诊肺部有无湿性啰音等。
● 心脏浊音界可正常,也可轻至中度扩大,心率多增快,少数也可减慢,心尖区第一心音减弱,可出现第四心音(心房性)奔马律,少数有第三心音(心室性)奔马律。
● 10%~20%患者在起病第2~3天出现心包摩擦音,为反应性纤维性心包炎所致,也需警惕亚急性心脏破裂风险[11]。
心尖区可出现粗糙的收缩期杂音或伴收缩中晚期喀喇音,为二尖瓣乳头肌功能失调或断裂所致。
室间隔穿孔时可在胸骨左缘3~4肋间新出现粗糙的收缩期杂音伴有震颤,可有各种心律失常。
对疑似STEMI的
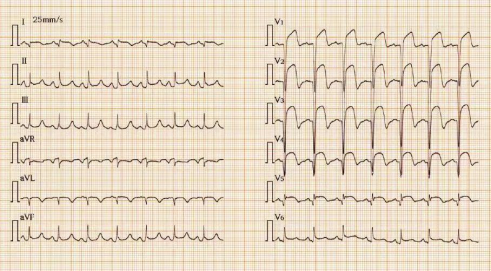
图1 STEMI患者的心电图(一)
STEMI的心电图表现为ST段弓背向上型抬高,呈单相曲线(图2),多形成病理性Q波或表现为R波减低,常伴对应导联镜像性ST段压低。
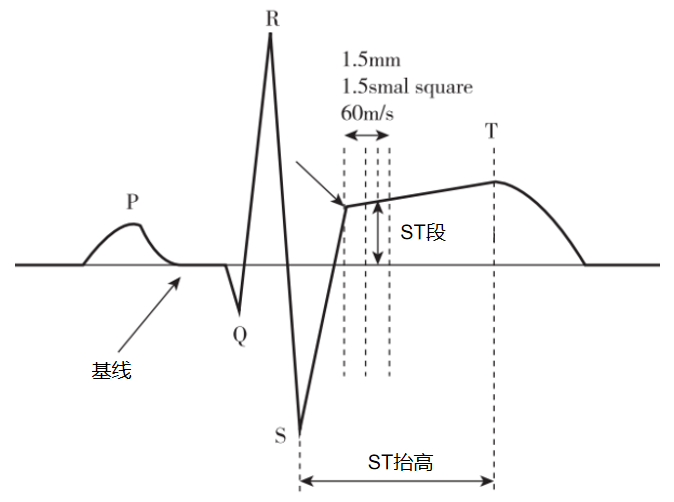
图2 STEMI的心电图(二)
注:图2中红色箭头标记的地方即为ST段抬高的表现
STEMI早期多不出现这种特征性改变,而表现为超急性T波(异常高大且两支不对称)改变和/或ST段斜直型升高,并发展为ST-T融合,伴对应导联的镜像性ST段压低。对于那些有持续
临床可根据ST段抬高的导联初步判断梗死部位,如前壁、下壁、右室等(表1)。
表1 STEMI心电图定位诊断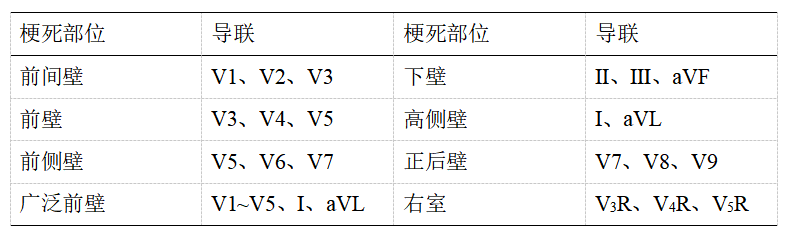
胸前导联必须相邻两个或两个以上导联,肢体导联两个或两个以上导联同时出现ST抬高和/或病理Q波,才能诊断心肌梗死。后壁梗死可伴随V1-3导联ST压低和/或r波升高,右室梗死V1导联可出现相应的变化。
心肌cTnI或cTnT是诊断心肌损伤最特异和敏感的标志物,cTn水平还与心肌坏死范围及预后明显相关。
推荐急性期常规检测cTn,如条件允许最好使用高敏cTn(hs-cTn)。无法检测cTn的情况下,也可以使用CK-MB质量法替代[11]。
普通cTn起病3~4小时后开始升高,cTnI于11~24小时达高峰,7~10天降至正常,cTnT于24~48小时达高峰,10~14天降至正常。
二维和M型
起病24~48小时后白细胞可增至(10~20)×109/L,中性粒细胞增多,嗜酸性粒细胞减少或消失;红细胞沉降率增快;
根据第四版“心肌梗死全球定义”[14],诊断STEMI需要同时满足急性心肌损伤(血清cTn升高)和新出现的缺血性心电图改变(ST段抬高)2项标准。
1.cTn升高的诊断标准
至少1次高于正常值上限(参考值上限值的99百分位值)。
2.ST段抬高的诊断标准[2]
相邻2个导联J点新出现ST段抬高,其中V2~V3导联≥2.5 mm(男性,<40岁);≥2 mm(男性,≥40岁);≥1.5 mm(女性,任何年龄);其他导联≥1.0 mm(图2)[14]。
风险评估及危险分层是一个连续的过程,有以下临床情况应判断为高危STEMI[13]:
● 高龄患者,尤其是老年女性。
● 存在严重的基础疾病,如糖尿病、心功能不全、肾功能不全、脑血管病、既往心肌梗死或
● 有重要脏器出血的病史,如
● 存在广泛面积的心肌梗死,包括广泛前壁心肌梗死、下壁合并右心室和/或正后壁心肌梗死、反复再发心肌梗死。
● 合并严重的并发症,如
● 院外
此外,也可通过心肌梗死溶栓治疗临床试验(the Thrombolysis in Myocardial Infarction,TIMI)评分对STEMI患者进行早期危险分层(表2)。
表2 TIMI危险评分系统
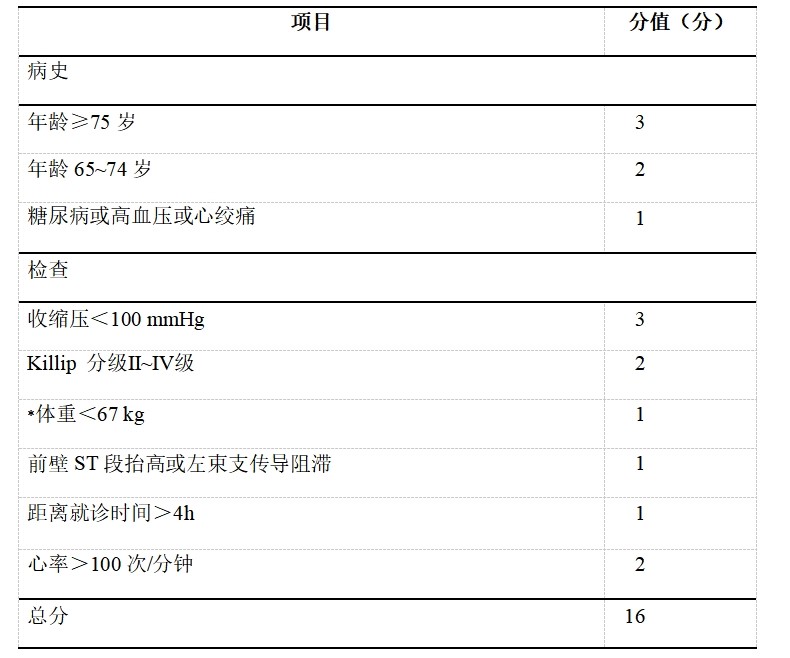
注:*此值为欧美数据,国人推荐以<50kg计分;TIMI 心肌梗死溶栓
根据TIMI评分总分进行危险分层,可分为:低危(0~3分),中危(4~6分)及高危(7~14分)。
(一)心力衰竭
心力衰竭不仅是STEMI最为常见的并发症,也是最重要的预后不良的指标之一[11]。应结合患者的症状、体征以及辅助检查结果尽早诊断,并采用Killip心功能分级进行描述。
根据有无心力衰竭表现及其相应的血流动力学损害程度,卧床STEMI患者发生的心力衰竭按Killip分级法可分为Ⅰ级~Ⅳ级(表3)。
表3 Killip心功能分级法[7]

(二)
STEMI患者
(三)心律失常
STEMI发病早期心律失常较为常见,且与预后密切相关,院前发生的室速及室颤是心脏性猝死的主要原因。早期再灌注治疗可减少室性心律失常和心血管死亡风险。
1.室性心律失常
室性心律失常是STEMI最常见的心律失常,导致血液动力学障碍的室速及室颤发生率约占6%~8%[7]。在STEMI急性期,预防性使用抗心律失常药物对患者是有害的。对于再灌注治疗中及STEMI发病24小时内发生的室性心律失常,是否需要进行干预治疗取决于其持续时间和对血液动力学的影响。对于无症状且不影响血液动力学的室性心律失常,不需要使用抗心律失常药物。而对于STEMI发病48小时后非缺血诱发的持续VT或VF,则是明显的预后不良指标,需评价是否有植入ICD的指征。对于反复发作VT和/或VF的STEMI患者,推荐早期进行完全血运重建,以解除潜在的心肌缺血。
对于合并多形性VT或VF的STEMI患者,如果没有禁忌证,应该静脉使用β受体阻滞剂进行治疗。对于反复出现多形性VT的患者,推荐静脉使用胺碘酮。如果经过多次电复律后血液动力学仍然不稳定并伴有反复发作VT的患者,也应该考虑静脉使用胺碘酮。如果β受体阻滞剂、胺碘酮和超速抑制治疗无效或无法获得,可以考虑使用利多卡因进行治疗。此外,还应注意纠正电解质紊乱,尤其是
对于经过完全血运重建和优化药物治疗后仍然反复发作室速、室颤或电风暴的STEMI患者,可以考虑在植入ICD后进行射频消融治疗[7]。
2.室上性心律失常
对于伴有
对于STEMI急性期新发
3.窦性心动过缓和
窦性心动过缓在下壁心肌梗死患者中较为常见,通常能够自行恢复且对预后无影响。对于这类患者,应进行密切监护,但一般不需要特殊处理。当STEMI患者出现
对于伴有血液动力学不稳定的窦性心动过缓或无稳定逸搏心律的高度
(四)机械并发症
多发生在STEMI早期,需及时发现和紧急处理。STEMI患者如有突发低血压、反复发作
1.游离壁破裂
游离壁破裂在AMI发病后的24小时内或1周左右较为常见,发生率低于1%,但病死率高达90%以上[7]。前壁心肌梗死是早期心脏破裂的主要发生部位,表现为循环“崩塌”,常在几分钟内死亡。老年、未能及时进行有效再灌注治疗以及延迟溶栓治疗是STEMI患者游离壁破裂的主要危险因素。游离壁破裂发生时,患者常出现突发的意识丧失和休克,检查结果可显示电机械分离以及急性
2.室间隔穿孔
室间隔穿孔可在STEMI发病后的24小时内出现,前壁和后外侧壁心肌梗死均可发生。其表现为临床情况迅速恶化,出现心力衰竭或
3.乳头肌或腱索断裂
乳头肌或腱索断裂导致的急性二尖瓣反流(MR)可能在STEMI发病后的2~7天出现。其表现为突发的急性左心衰竭、血液动力学不稳定、肺
STEMI应与急性肺动脉栓塞、
主要临床表现包括
● 血
● 血气分析多为低氧及低二氧化碳。
●
● 肺动脉CTA可明确诊断。
一般表现为剧烈
一般表现为持久而较剧烈的
ECG除aVR导联外,其余导联均有ST段弓背向下抬高,T波倒置,通常无异常Q波出现;结合心脏超声,可协助诊断。
通常表现为
胸部 X 线或 CT 检查可明确诊断。
结合ECG和血清
易误诊人群
老年、女性和糖尿病患者,
本病被误诊为其他疾病
● 本病部分患者疼痛部位不在胸部,而位于上腹部,可被误认为胃病、
● 部分患者表现为嗓子痛、咽部灼热感而被误诊为急性咽炎或喉炎。
● 或疼痛放射至下颌、颈部、背部上方,被误认为牙痛或骨关节痛。
但这些疾病均不会出现STEMI的心电图特征性改变和演变过程。
其他疾病被误诊为本病
以
避免误诊的要点
仔细询问病史,及早并反复多次做心电图检查,化验
在正常人群中预防动脉粥样硬化和冠心病属一级预防,冠心病和心肌梗死患者需采取二级预防措施,以预防再次发生梗死和其他心血管事件。ABCDE方案可指导二级预防:
A:采用抗血小板药物、抗心绞痛治疗以及血管紧张素转换酶抑制剂;
B:应用β受体阻滞剂来预防心律失常、减轻心脏负荷,并控制血压;
C:控制血脂水平和戒烟;
D:控制饮食和进行糖尿病治疗;
E:进行健康教育和运动。
基于运动的心脏康复可以降低STEMI患者的全因死亡率和再梗死的风险,同时有助于更好地控制危险因素、提高运动耐力和生活质量。对于符合条件的患者,建议在住院期间尽早开始康复治疗。
出院前进行运动负荷试验,以客观评估运动能力,并为日常生活或制定运动康复计划提供指导。
早期进行心肺运动试验在安全性和临床价值方面表现良好[26]。
建议病情稳定的患者每天进行30~60分钟中等强度的有氧运动(例如快步行走),每周至少5天,并逐渐增加抗阻训练。运动锻炼应该循序渐进,避免诱发心绞痛和心力衰竭。
患者出院第1/3/6个月前往门诊复诊,复查心电图、心脏彩超、血常规、肝肾功能、电解质、心肌标志物,之后每年复查一次,不适随诊。
出院后要坚持长期药物治疗,控制缺血症状、降低心肌梗死和死亡的发生,包括服用双联抗血小板药物至少12个月,其他药物包括他汀类药物、β受体拮抗剂和ACEI/ARB,严格控制危险因素,进行有计划及适当的运动锻炼。根据住院期间的各种事件、治疗效果和耐受性,予以个体化指导治疗。
本站内容仅供医学专业人士参考
不能作为诊断及医疗依据,请谨慎参阅
©医知源 版权所有,未经许可,不得以任何形式对医知源内容和插图进行转载使用。






 长按文字
长按文字